En el mundo de los ensayos clínicos, la cuestión no es si se enfrentará a una inspección, sino cuándo. Tanto si es un centro, un patrocinador o CRO, mantener la preparación para las inspecciones no es solo una cuestión de cumplimiento normativo, sino también de proteger la seguridad de los participantes y garantizar la integridad de los datos. Veamos qué se necesita para responder con confianza «sí» cuando llamen a la puerta.
¿Qué es la preparación para la inspección?
La preparación para la inspección es un estado de preparación continuo que garantiza el cumplimiento de los marcos normativos, incluidos los requisitos de la ICH-GCP, las normativas de la FDA (21 CFR Partes 11, 50, 54 y 312), el Reglamento (UE) n.º 536/2014 sobre ensayos clínicos, el RGPD, los requisitos de la MHRA GCP, las directrices de la OMS sobre BPC y otras normas aplicables. Es la base que protege la seguridad y el bienestar de los participantes, al tiempo que garantiza el cumplimiento de los protocolos de los estudios.
Hay mucho en juego. Según los datos de inspección de la FDA de 2024, el incumplimiento de los protocolos representa el 55,4 % de las citaciones de los investigadores, mientras que los registros inadecuados del historial de los casos representan el 24,1 % de los hallazgos. Estas estadísticas ponen de relieve una verdad fundamental: estar preparado no solo es una buena práctica, sino que es esencial para mantener la integridad de los datos y evitar costosos retrasos.
Comprender el proceso de inspección
Aunque los procedimientos de inspección varían según la autoridad reguladora, varios elementos clave siguen siendo los mismos:
- Notificación formal de la autoridad reguladora anunciando la próxima inspección.
- Reunión inicial para establecer el alcance y definir expectativas claras.
- Solicitudes de documentos realizadas antes, durante o después de la inspección.
- Solicitudes de acceso al sistema que van desde la visualización por encima del hombro hasta el acceso directo a través de cuentas de inspector dedicadas.
Comprender este proceso ayuda a las organizaciones a prepararse de forma sistemática en lugar de actuar con precipitación cuando llega la notificación.
La ventaja tecnológica: por qué son importantes los sistemas electrónicos
Los días de rebuscar en archivadores y carpetas durante las inspecciones están contados. Los sistemas electrónicos han transformado la preparación para las inspecciones, pasando de ser una pesadilla logística a un proceso optimizado.
Consideremos la diferencia práctica: un inspector solicita todos los informes de eventos adversos de los últimos seis meses. Con los sistemas en papel, esto implica buscar en múltiples carpetas, con la posibilidad de perder documentos y consumir un valioso tiempo de inspección. Con un sistema electrónico como CRIO, es cuestión de unos pocos clics: instantáneo, completo y auditable.
Los sistemas electrónicos ofrecen claras ventajas:
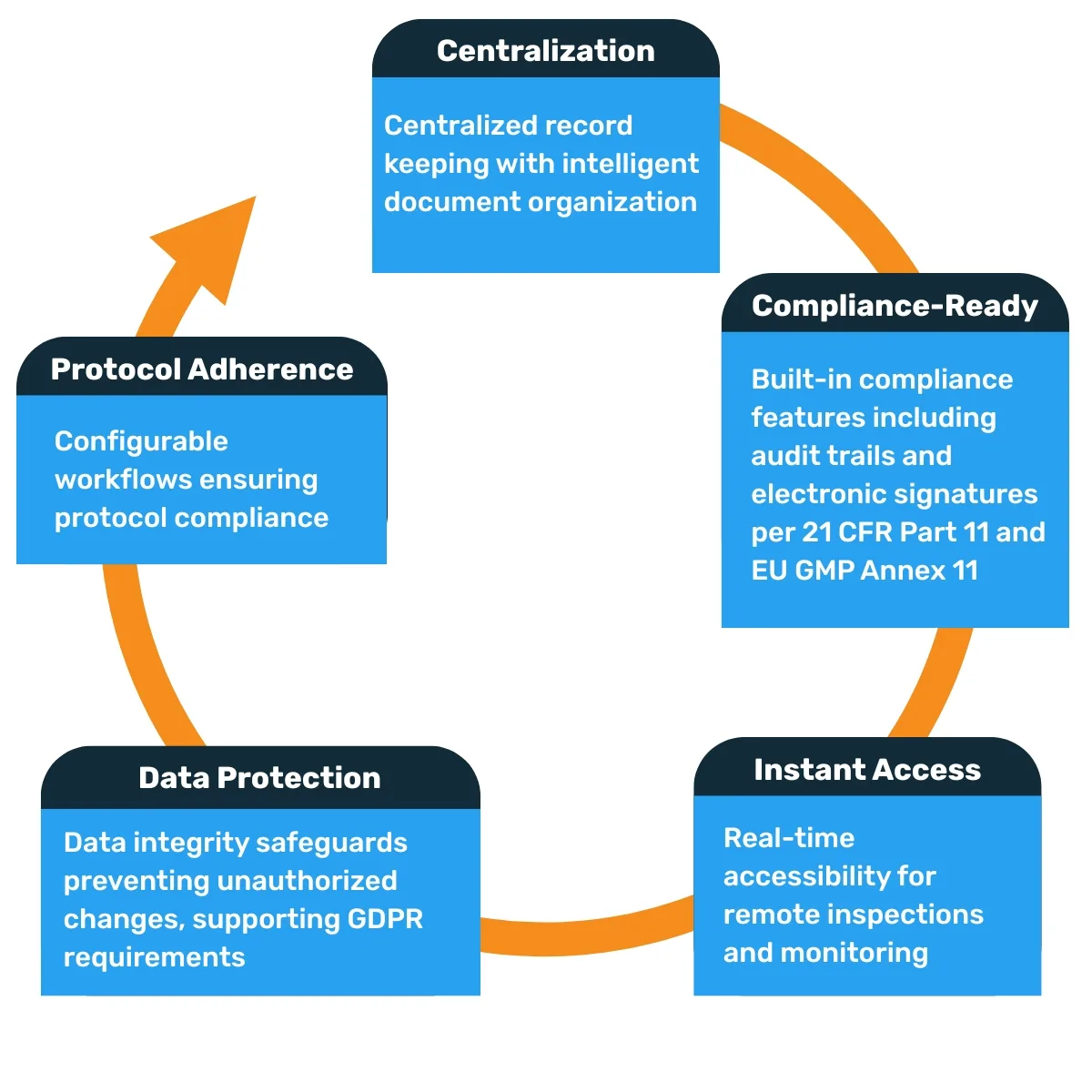
Aceptando la evolución normativa
El panorama normativo ha evolucionado drásticamente, especialmente tras la pandemia. Las directrices de la FDA sobre evaluación normativa remota (RRA) y la ICH E6(R3) demuestran la aceptación por parte de los organismos reguladores de la tecnología y los enfoques basados en el riesgo.
Principios clave de la ICH E6(R3) que respaldan la adopción de tecnología:
- Neutralidad de los medios: elija el sistema electrónico que mejor se adapte a su organización.
- Flexibilidad e innovación: Aprovecha los dispositivos portátiles, la monitorización remota y los enfoques novedosos.
- Calidad proactiva: integrar la calidad en los procesos desde el principio.
- Gobernanza de datos: garantizar la recopilación, el almacenamiento y el acceso responsables de los datos de conformidad con el RGPD (cuando proceda).
- Proporcionalidad del riesgo: Equilibrar la supervisión con la eficiencia operativa
Como señaló recientemente Jason Wakelin-Smith, de la MHRA: «Es hora de compañías farmacéuticas adopten la proporcionalidad del riesgo, sabiendo que cuentan con el apoyo de los reguladores para su uso».
Los nueve pilares de la preparación para la inspección
La verdadera preparación para la inspección requiere excelencia en nueve áreas críticas:
1. Cumplimiento normativo
Cumplir con las regulaciones de la FDA (21 CFR Partes 11, 50, 54 y 312), las directrices de la EMA, los requisitos de BPC de la MHRA, las directrices de BPC de la OMS, las directrices ICH-GCP y otros marcos aplicables. No se trata solo de conocer las regulaciones, sino de demostrar su aplicación coherente.
2. Documentación del estudio
Mantenga registros completos, precisos y actualizados, incluidos los archivos del centro investigador (ISF), los documentos originales y los CRF, de conformidad con los requisitos de la norma 21 CFR Parte 312. La documentación debe reflejar el historial completo de su ensayo.
3. Formación y delegación
Asegúrese de que todo el personal esté debidamente capacitado, con registros documentados y registros claros de delegación, de conformidad con la norma 21 CFR Parte 312. Todos los miembros del equipo deben comprender sus responsabilidades y limitaciones.
4. Seguridad y derechos de los participantes
Implemente procesos sólidos de consentimiento informado que cumplan con la norma 21 CFR Parte 50 y mantenga sistemas que prioricen la seguridad de los participantes por encima de todo. Asegúrese de documentar adecuadamente los intereses financieros según la norma 21 CFR Parte 54.
5. Gestión de productos en fase de investigación
Mantenga un almacenamiento seguro con controles de temperatura adecuados y registros de responsabilidad meticulosos. Cada dosis debe ser trazable desde su recepción hasta su eliminación, de acuerdo con los requisitos de la norma 21 CFR Parte 312.
6. Integridad de los datos
Garantizar la introducción de datos precisa y oportuna, la resolución rápida de consultas y registros de auditoría completos que cumplan con las normas 21 CFR Parte 11 y el Anexo 11 de las BPF de la UE. Los datos deben cumplir con ALCOA+: atribuibles, legibles, contemporáneos, originales, precisos, además de completos, coherentes, duraderos y disponibles. El tratamiento de los datos personales debe ajustarse a los requisitos del RGPD (cuando sea aplicable).
7. Preparación operativa
Establezca procesos claros para gestionar las inspecciones con documentación fácilmente accesible. Su equipo debe saber exactamente qué hacer cuando lleguen los inspectores.
8. Garantía de calidad
Realizar auditorías internas periódicas, aplicar eficazmente el sistema CAPA y mantener enfoques de supervisión basados en el riesgo que sean coherentes con las directrices ICH E6(R3) y GCP de la OMS.
9. Tecnología y sistemas
Utilice sistemas validados con una supervisión adecuada por parte del proveedor y pruebas de aceptación por parte del usuario documentadas. Su tecnología debe mejorar, y no obstaculizar, el cumplimiento de los principios del título 21 del CFR, parte 11, y del anexo 11 de las buenas prácticas de fabricación de la UE.
Pasos prácticos para lograr la preparación
Ponga en práctica estos principios con los siguientes pasos prácticos:
Crear un plan de preparación del sitio: Desarrollar una lista de verificación exhaustiva que cubra todos los documentos esenciales. Asignar responsabilidades claras para el mantenimiento de cada aspecto de la preparación para la inspección.
Implemente un sistema centralizado: ya sea físico o electrónico, mantenga un sistema de archivo organizado que permita recuperar rápidamente cualquier documento que pueda solicitar un inspector.
Realice simulacros de inspección: Las simulaciones periódicas permiten identificar deficiencias y reforzar la confianza del equipo. Tómelas en serio, ya que son la mejor preparación para la situación real.
Establecer un equipo de respuesta a la inspección: designar un responsable de la inspección y crear protocolos de comunicación claros. Todos deben conocer su función cuando llegue el día de la inspección.
Adopte la mejora continua: utilice los resultados de las inspecciones, ya sean simuladas o reales, como oportunidades de aprendizaje para reforzar sus procesos.
Consideraciones fundamentales para el éxito

Cómo evitar dos errores críticos
Error n.º 1: Supervisión inadecuada de los proveedores No dé por sentado que su proveedor cumple con la normativa: compruébelo. Solicite documentación completa sobre el cumplimiento de la norma 21 CFR Parte 11, el Anexo 11 de las BPF de la UE y el RGPD antes de la implementación, no durante una inspección.
Escollo n.º 2: Procesos internos deficientes. Disponer de una tecnología excelente no sirve de nada sin unos procesos claros para utilizarla. Elabore unas directrices exhaustivas para el personal y mantenga pruebas de que los sistemas funcionan según lo previsto.
El resultado final
La preparación para las inspecciones no es un destino, sino un viaje de mejora continua. Al adoptar herramientas electrónicas que cumplen con las normas 21 CFR Parte 11 y el Anexo 11 de las BPF de la UE, mantener una documentación completa y fomentar una cultura de calidad alineada con las directrices de buenas prácticas clínicas, usted transforma las inspecciones de eventos temidos en oportunidades para mostrar su excelencia.
Recuerde que, en esencia, la preparación para la inspección se basa en dos principios fundamentales: proteger a los participantes en el estudio (21 CFR Parte 50) y garantizar la integridad de los datos (21 CFR Parte 11, RGPD). Todo lo demás contribuye a estos objetivos fundamentales.
La pregunta sigue siendo: ¿Estás listo para una inspección de ensayo clínico mañana?
Con una preparación adecuada, la tecnología adecuada y el compromiso con estos principios, puedes responder con confianza «sí» no solo mañana, sino todos los días.
En CRIO, hemos incorporado la preparación para inspecciones como parte fundamental de nuestra plataforma. Nuestro completo centro de documentación, los certificados de validación y las funciones de cumplimiento integradas ayudan a Clinicas, compañías farmacéuticas y las CRO a mantener la preparación para inspecciones como un estado continuo, y no como una tarea de última hora. Obtenga más información sobre cómo lograr la preparación para inspecciones con CRIO en clinicalresearch.io.
