Su plataforma eSource compatible con la norma 21 CFR Parte 11
Es fácil suponer que los datos de investigación clínica se encuentran en los registros médicos electrónicos (EHR) y que solo hay que transferirlos al sistema de captura electrónica de datos (EDC). Sin embargo, los datos de investigación suelen acabar en documentos en papel, ya que los sistemas EHR están diseñados para capturar registros relacionados con diagnósticos y atención al paciente, no con la investigación.
Existe un software de investigación clínica probado que puede cerrar esta brecha y aliviar la carga que supone llevar a cabo investigaciones dentro de su institución. Se trata, sin duda, de CRIO.
-
40% menos de desviaciones del protocolo
-
Riesgo de auditoría un 70% menor
Profundice en las diferencias entre EHR y eSource y descubra cómo CRIO salva las distancias.
Software intuitivo para la investigación clínica que permite un cumplimiento eficiente de los protocolos
CRIO, una tecnología de gestión electrónica de fuentes (eSource) extraordinariamente sencilla creada por un equipo de expertos en investigación clínica, te ayuda a prescindir del papel, a sacar el máximo partido a los sistemas con los que ya cuentas y a potenciar a tus equipos.
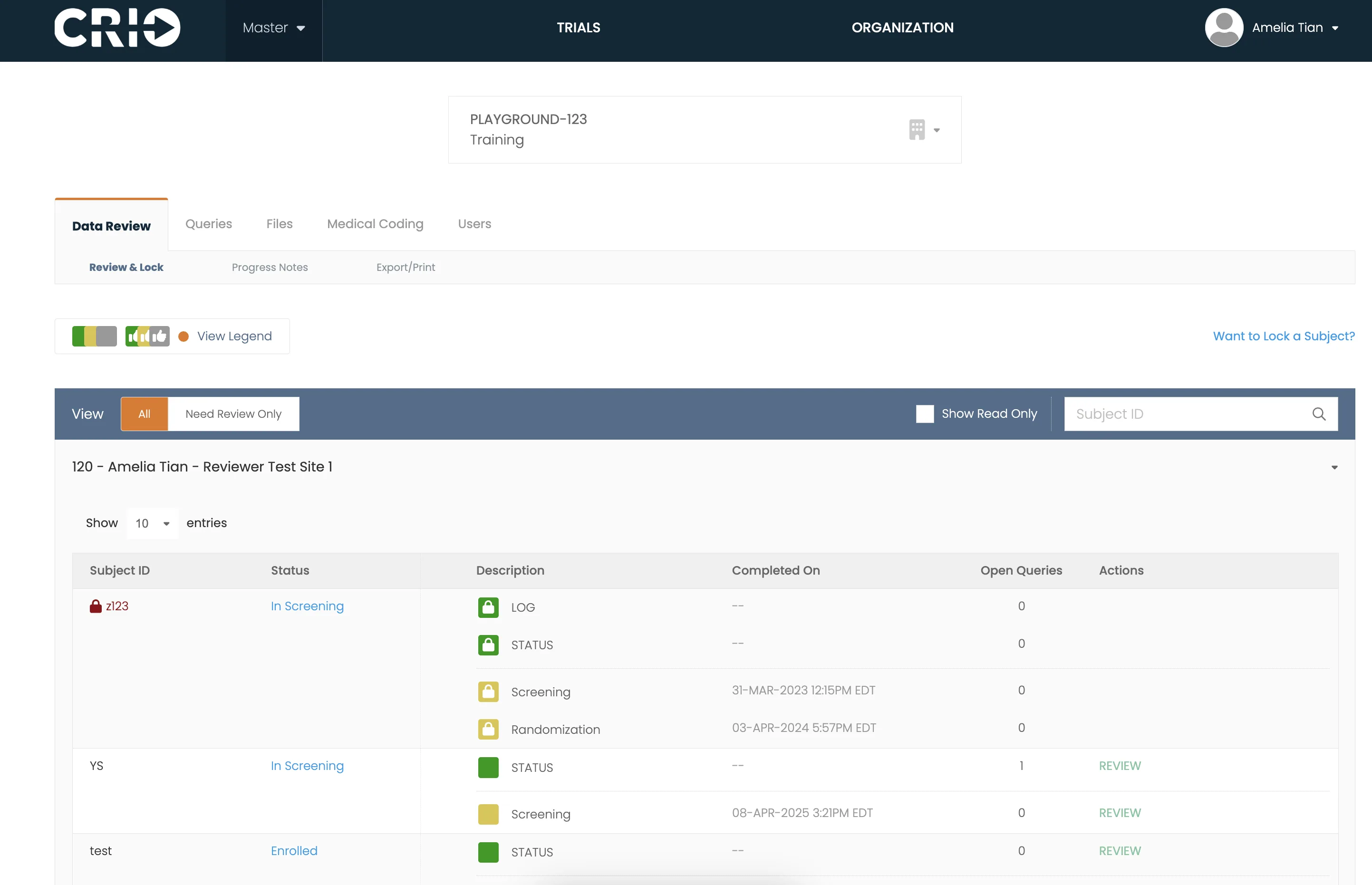
Colaborar de forma remota
- Reducir las diferencias entre los sistemas de historias clínicas electrónicas, los documentos originales en papel y la recopilación electrónica de datos
- Optimizar la revisión de los datos de laboratorio y los registros médicos por parte del investigador principal (IP).
- Proporcionar una supervisión remota cómoda para los asistentes de investigación clínica (CRA) y reducir la carga de trabajo de los coordinadores.
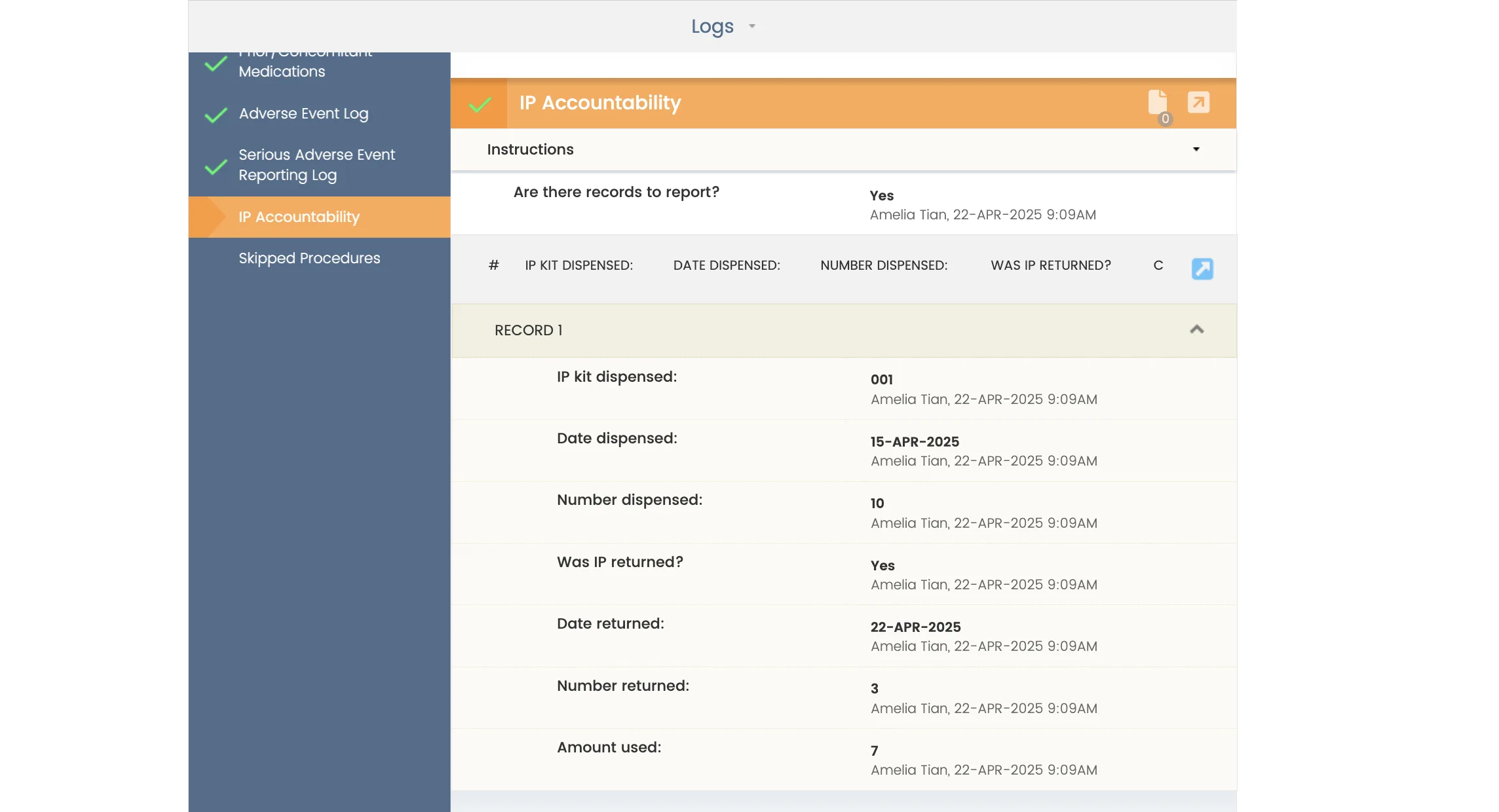
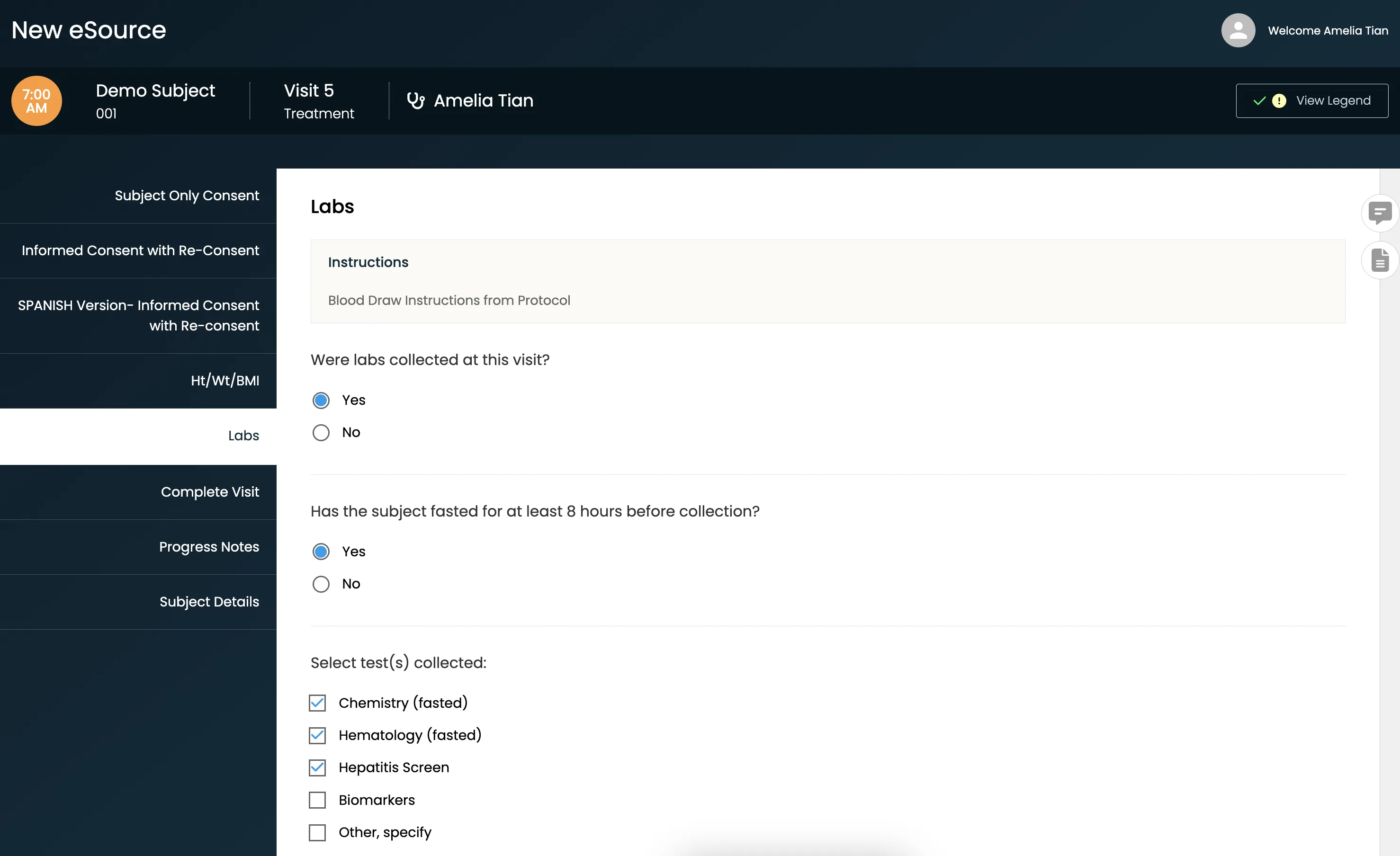
Realice fácilmente ensayos clínicos iniciados por investigadores con EDC integrado
- Configure y despliegue rápidamente plantillas eSource sin necesidad de programación.
- Rellene automáticamente el EDC con datos protegidos por la PHI a medida que completa las plantillas de origen, eliminando la transcripción y la verificación de datos de origen (SDV).
- Admite ensayos únicos y multisitio, incluidos aquellos que requieren el cumplimiento de la norma 21 CFR Parte 11.
Salvaguardar la seguridad y la calidad
- Cumpla con las directrices de cumplimiento, incluida la norma 21 CFR Parte 11.

Estudio de caso
Esta universidad ahorra más de 650 horas de trabajo de coordinación al año.
Descubra qué sucede cuando los centros de investigación académica dejan de usar papel gracias al software CRIO eSource.