El ecosistema de la investigación clínica ha experimentado un aumento en la complejidad de los protocolos que está imponiendo una carga operativa sin precedentes a Clinicas de investigación Clinicas concretamente, está poniendo a prueba su capacidad para crear plantillas de diseño de estudios.
El creciente desafío de la complejidad de los protocolos
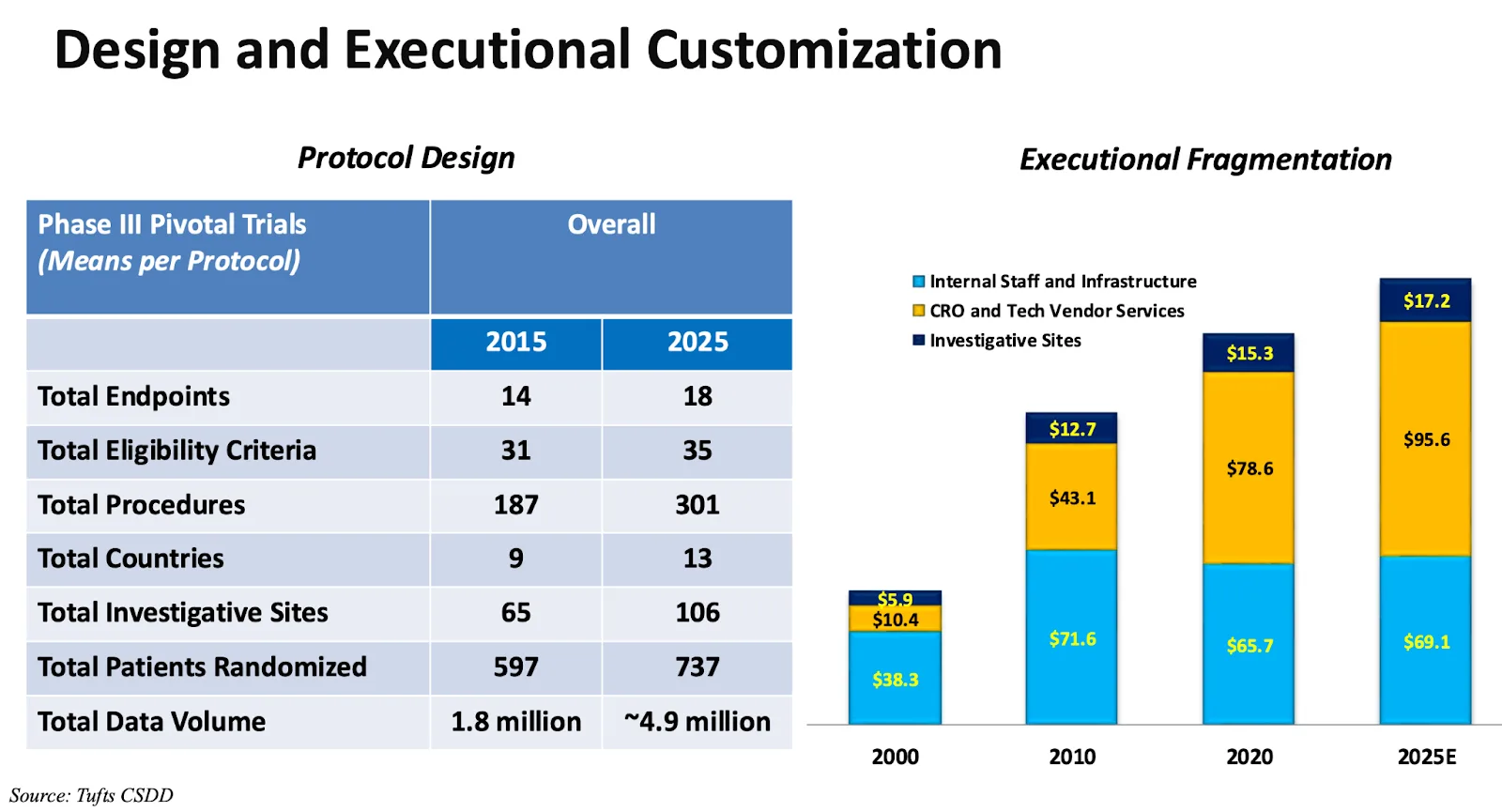
Los datos del CSDD de Tufts han puesto de relieve recientemente cómo los protocolos siguen ampliando sualcance1. Entre 2015 y 2025, los ensayos fundamentales de fase III han registrado:
- Los procedimientos aumentan en más de un 60 % (de 187 a 301).
- Clinicas de investigación Clinicas más de un 60 % (de 65 a 106).
- Los puntos finales aumentan en un 30 % (de 14 a 18).
- Los criterios de elegibilidad aumentan en más de un 10 % (de 31 a 35).
- El volumen de datos casi se triplicó (de 1,8 millones a 4,9 millones de puntos de datos).
Igualmente importante es que los datos de Tufts muestran que las modificaciones y desviaciones del protocolo también han aumentado considerablemente. Más recientemente, los ensayos de fase III tienen ahora una media de 3,5 modificaciones por ensayo, lo que supone un aumento de más del 50 % con respecto a hace cinco años, y el ensayo medio tiene 296 desviaciones del protocolo, casi el triple que hace diez años.
Evidencia desde el terreno: servicios de diseño de estudios en la práctica
Toda esta complejidad de los protocolos tiene importantes repercusiones en Clinicas de investigación, que deben traducir estos protocolos en plantillas de diseño de estudios, es decir, hojas de trabajo detalladas con instrucciones y campos de datos obligatorios para guiar la recopilación de datos conforme al protocolo. Una plantilla de diseño en blanco en papel puede tener entre 5 y 15 páginas por visita del estudio; un estudio con 10 visitas podría fácilmente superar las 100 páginas.
En CRIO, contamos con un servicio especializado en diseño de estudios que ha creado más de 1600 plantillas electrónicas en nombre de nuestros clientes. Esto nos proporciona una perspectiva única sobre cómo se manifiesta la complejidad de los protocolos a nivel de centro.
Utilizando nuestra metodología interna de puntuación y control de calidad, que tiene en cuenta factores como visitas, brazos, esquemas, ciclos y eCRF, hemos observado un aumento constante en la complejidad del diseño de los estudios desde 2018. Hasta 2024, el número medio de procedimientos por estudio ha crecido aproximadamente un 55 % en los últimos seis años, una tendencia en línea con el aumento del 60 % calculado por Tufts para los últimos diez años.
En otras palabras, dos puntos de vista muy diferentes conducen a la misma realidad: los protocolos son cada vez más complejos y la carga se está trasladando a Clinicas.2
La inversión de tiempo detrás de cada construcción
La complejidad no es solo un concepto abstracto, sino que tiene un coste medible en tiempo. Nuestros equipos de diseño de estudios tardan una media de 33 horas en crear una plantilla eSource para un solo estudio (incluido el control de calidad adecuado tras el diseño). Eso supone casi una semana completa del tiempo de un coordinador, tiempo que, de otro modo, podría dedicarse a la atención y la inscripción de pacientes. Esta carga es bastante similar en todas las áreas terapéuticas; consulte las métricas de tiempo medio de CRIO por área terapéutica a continuación.
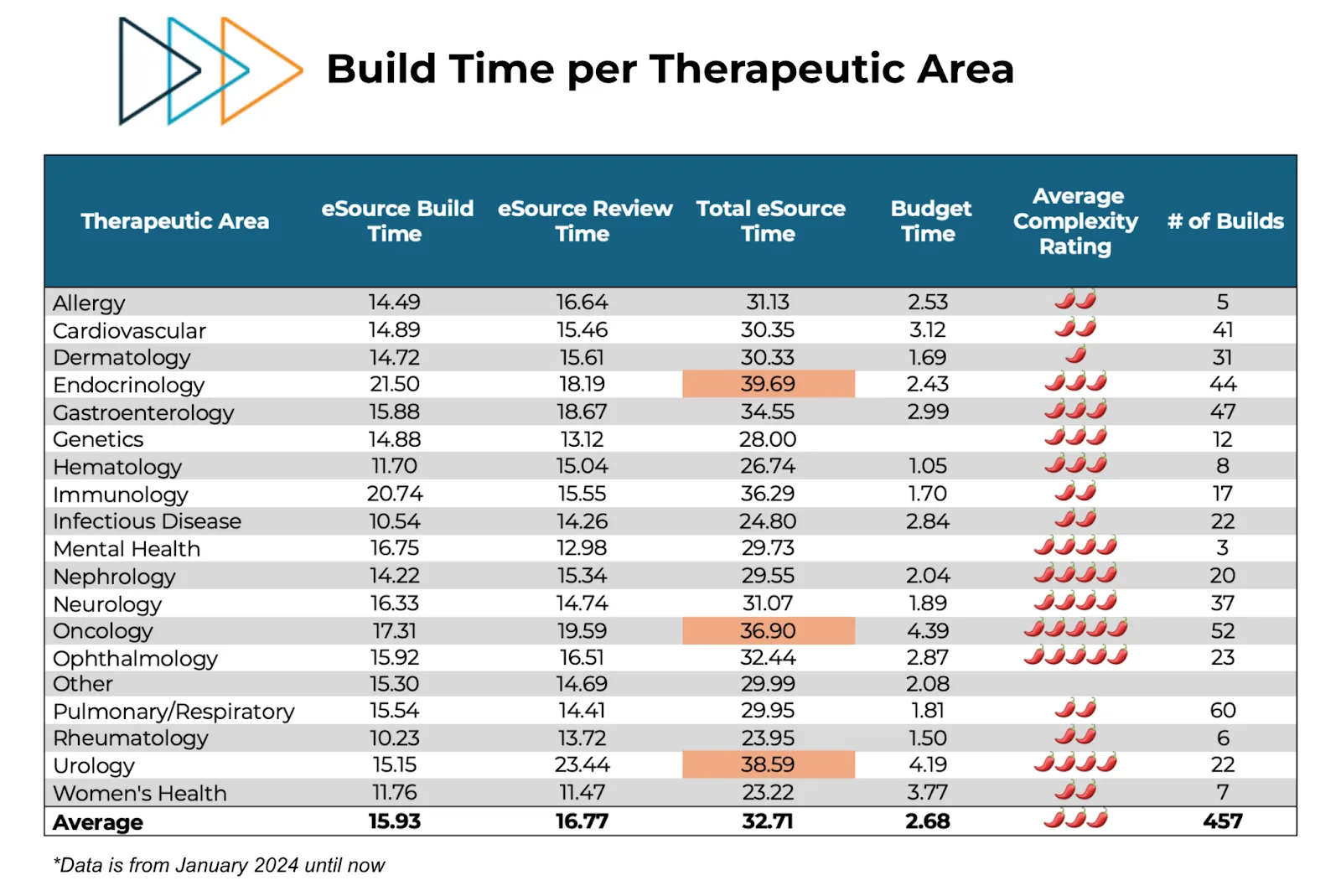
Y eso es solo el tiempo facturable. El tiempo transcurrido suele ser mayor, ya que los coordinadores, que están muy ocupados, tienen que encajar este tiempo en su semana laboral. Como resultado, la inscripción suele retrasarse, ya que Clinicas para finalizar las construcciones antes de poder atender a los pacientes. De hecho, la experiencia de CRIO es que cuando Clinicas proporciona a Clinicas una plantilla eSource preconstruida y diseñada de forma centralizada, inscriben a los pacientes entre 30 y 45 días más rápido. Esto implica que el centro medio necesita un mes de tiempo transcurrido para completar la construcción del estudio.
El impacto en Clinicas
La creciente complejidad se traduce en retos muy tangibles para Clinicas:
- Carga de trabajo y agotamiento del personal: los coordinadores pasan semanas sumergidos en tareas de desarrollo, lo que retrasa las tareas relacionadas con los pacientes. La formación de nuevo personal en desarrollos cada vez más complejos agrava el problema. Clinicas se enfrentan a una escasez de coordinadores de investigación con experiencia.
- Retrasos en la inscripción: como se ha mencionado anteriormente, las más de 30 horas que se tarda en preparar un estudio provocan retrasos de entre 4 y 6 semanas antes de que Clinicas empezar a atender a los pacientes.
- Aumento de las desviaciones del protocolo y la repetición del trabajo: los protocolos más complejos dificultan el diseño de plantillas de estudio exhaustivas que sirvan de guía para el trabajo de los coordinadores. El aumento de casi tres veces en las desviaciones del protocolo por estudio es un síntoma claro y llamativo.
- Riesgos de auditoría y cumplimiento: un mayor número de modificaciones y desviaciones aumenta los resultados de las auditorías y la exposición a la normativa. Cada ciclo de reelaboración crea oportunidades para que se produzcan errores que comprometan la integridad de los datos.
- Carga de supervisión: un mayor número de errores y reelaboraciones también aumenta la carga de supervisión. Son ellos quienes deben realizar la «revisión de los datos de origen», garantizando la precisión y la coherencia de los datos. A menudo, se necesitan dos ciclos de visitas de supervisión, hasta 12 semanas, para completar revisiones satisfactorias de los datos de origen.
Mirando hacia el futuro: la necesidad de un diseño de estudio maduro y optimizado
La complejidad de los protocolos no va a cambiar. Las terapias personalizadas, las enfermedades raras y la oncología seguirán impulsando el aumento de la demanda. Sin un cambio drástico de paradigma, la creciente carga que supone el diseño de los estudios seguirá ralentizando los ensayos.
Un cambio de paradigma es Central eSource. En lugar de Clinicas creen sus propias plantillas de origen Clinicas y luego vuelvan a introducir manualmente los datos de origen en el EDC, compañías farmacéuticas proporcionar Clinicas una plantilla eSource estandarizada y basada en protocolos que incorpora calidad en el punto de captura. Dado que la plantilla de origen está diseñada de forma centralizada, se puede asignar directamente al EDC, lo que permite una integración a gran escala. Clinicas entonces utilizar la interfaz EDC exclusiva de CRIO para enviar los datos directamente al EDC, lo que elimina la introducción manual.
Al igual que Central IRB estandarizó y optimizó el proceso ICF, Central eSource aplica el mismo modelo al diseño de fuentes. En lugar de que 50 Clinicas 50 plantillas, lo que supone literalmente un año completo de trabajo a más de 30 horas por centro, un equipo de diseño centralizado crea una plantilla optimizada, en consonancia con el EDC, que luego se comparte entre Clinicas Al igual que con la plantilla del ICF, Clinicas realizar la configuración específica del centro según sea necesario. Este equilibrio crea un «núcleo» estandarizado básico necesario para la integración del EDC, rodeado de una «cubierta» flexible que admite los procedimientos operativos estándar locales, las prácticas institucionales y las preferencias del personal.
El resultado es la estandarización entre Clinicas, una mayor calidad de los datos y un tiempo de inscripción más rápido. compañías farmacéuticas coherencia, Clinicas tener que realizar construcciones aisladas tediosas y propensas a errores, y ambas se benefician de la calidad integrada en el punto de captura, un tiempo más rápido para la entrada en EDC y una monitorización remota más flexible y basada en el riesgo. En resumen, Central eSource sustituye docenas de plantillas creadas in situ por un único diseño de alta calidad que reduce los riesgos, los retrasos y los costes.
Conclusión
Los datos del equipo de diseño del estudio de Tufts y CRIO pintan un panorama claro, coherente e inequívoco: los protocolos son cada vez más complejos y la carga que soportan Clinicas creciendo a un ritmo insostenible. Si no se aborda, esta tendencia seguirá retrasando las inscripciones, aumentando las desviaciones de los protocolos y agotando los ya escasos recursos de los centros.
Estamos llegando a un punto crítico. La industria debe explorar nuevas soluciones para mantener la viabilidad de los ensayos. Central eSource no solo es un modelo probado para aliviar la carga de los centros, sino que también es una forma de dar Clinicas influencia, más flexibilidad y más eficiencia, mientras que compañías farmacéuticas de datos más limpios y estandarizados.
1Fuente: Ken Getz, Tufts CSDD, discurso inaugural de la Cumbre sobre la Evolución, mayo de 2025.
2Fuente: CRIO, Historial del diseño del estudio – Primer trimestre de 2025.
