Se ha escrito mucho sobre la iniciativa eSource-to-EDC y, aunque la iniciativa Central eSource de CRIO contribuye significativamente a esta tendencia, el verdadero valor de eSource va más allá de la simple captura de datos para completar el EDC.
compañías farmacéuticas tres beneficios específicos de Central eSource, además de la aceleración de la introducción de datos y la reducción de la necesidad de SDV gracias a la integración con el EDC.
1. Central eSource promueve el cumplimiento del protocolo.
El EDC es una herramienta de entrada secundaria, por lo que ninguna de las comprobaciones de edición promueve el cumplimiento del protocolo en sí mismo, sino que son meras herramientas para garantizar la introducción precisa y completa de los datos a partir de los datos de origen ya recopilados.
Por el contrario, eSource implica la captura simultánea de datos mientras se lleva a cabo el procedimiento. Por este motivo, las comprobaciones de edición en eSource promueven el cumplimiento del protocolo, ya que proporcionan información en tiempo real para guiar al centro en el proceso de recopilación de datos.
Los datos de eSource son más amplios que los datos de EDC, ya que eSource, cuando se escribe correctamente, contiene las instrucciones de flujo de trabajo establecidas en el protocolo. Al garantizar que el centro recopila los datos de forma estandarizada, tal y como indica el protocolo, eSource asegura que el subconjunto de datos que se asigna al eCRF sea realmente comparable con los datos recopilados por otras Clinicas.
El siguiente diagrama muestra de forma visual cómo eSource abarca datos procedimentales y de cumplimiento, y no solo los datos finales que suelen asociarse con el eCRF:
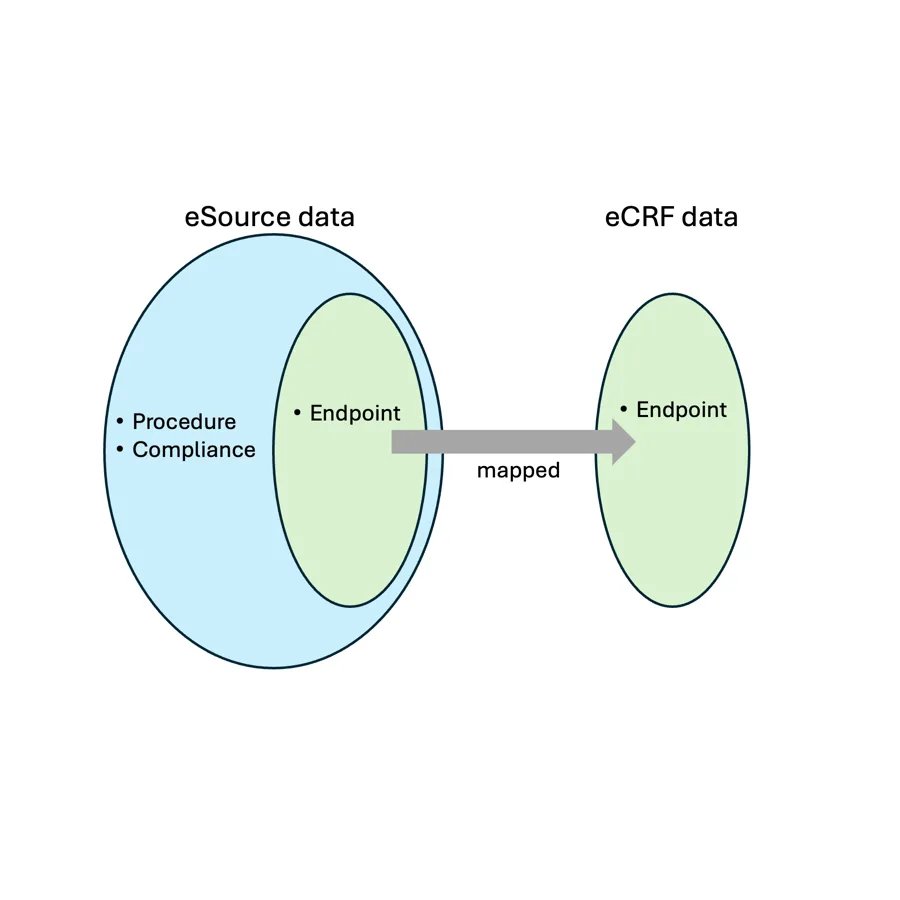
2. Central eSource facilita la puesta en marcha del sitio y la inscripción.
Cuando un centro recibe el protocolo del patrocinador tras ser seleccionado para un estudio, debe traducirlo a un conjunto de hojas de trabajo originales. En papel, estas hojas de trabajo pueden ocupar 10 páginas para una sola visita; un estudio con 10 visitas podría fácilmente dar lugar a más de 100 páginas de hojas de trabajo que deben completarse.
Huelga decir que se trata de un proceso que requiere mucho tiempo. La experiencia de CRIO, tanto con su propio trabajo de diseño de eSource como con las conversaciones con Clinicas, es que un coordinador de investigación puede dedicar hasta 35 horas a redactar plantillas de fuentes completas. Se trata del tiempo facturable, no del tiempo transcurrido; huelga decir que encontrar el tiempo para dedicarle puede ser todo un reto.
Como resultado, un estudio de caso sobre Central eSource mostró que Clinicas optaron por utilizar CRIO inscribieron a su primer paciente 41 días antes que Clinicas decidieron no hacerlo, lo que representa aproximadamente 7 semanas, lo que podría explicarse fácilmente por el retraso incremental que tardan Clinicas «poner en marcha» la fuente.
Por supuesto, Clinicas podrían comenzar la compilación de la fuente antes de la visita de inicio del sitio, pero muchas optan por no hacerlo, ya que saben por experiencia que estudios retrasarse y retirarse, y muy pocas Clinicas dispuestas a invertir en exceso en el tiempo de preparación del estudio antes de que se firme el acuerdo de ensayo clínico.
A menos que el estudio tenga un período de inscripción previsto muy corto (como un estudio sobre la vacuna contra la gripe), Clinicas pocos incentivos para acelerar su calendario.
El mismo estudio de caso que demostró que Clinicas más rápido también demostró que inscriben más, un 40 % más de media. Esto no es sorprendente, dado que una inscripción más temprana debería traducirse en una mayor inscripción general, ya que amplía el plazo de reclutamiento para Clinicas proporciona al centro una experiencia fundamental que comprime su curva de aprendizaje.
3. Central eSource facilita la supervisión remota: la introducción más rápida de datos electrónicos no
Incluso con la llegada de la supervisión basada en el riesgo, la supervisión del centro representa una parte significativa del presupuesto total de un estudio. Además de la verificación de los datos originales, los supervisores también realizan una revisión de los datos originales (SDR), que es la revisión independiente de la fuente de un centro para comprobar la coherencia de la documentación, la supervisión del PI y el cumplimiento del protocolo y la ICH-GCP.
El SDR es una actividad fundamental que descubre desviaciones del protocolo que pueden no ser evidentes en el EDC. Por ejemplo, el SDR puede revelar cualquiera de los siguientes hallazgos, todos los cuales pueden socavar la integridad de los datos del estudio:
- Condiciones médicas no reveladas (por ejemplo, a partir de una nota de evolución, valores de laboratorio, etc.) que indiquen que un paciente ha sido aleatorizado de forma incorrecta.
- Falta de supervisión del investigador principal, como la falta de participación del investigador principal en la documentación crítica, como la elegibilidad, el historial médico o la revisión de eventos adversos.
- Realización incorrecta de un procedimiento, como una nota de fuente que muestra que los datos finales no se recopilaron de la manera requerida por el protocolo.
- Realización de un procedimiento por parte de un miembro del personal que no ha sido debidamente delegado y/o formado (ya que la atribución de la fuente no es evidente en el EDC).
El SDR es una tarea que requiere mucho tiempo y, con una cadencia de supervisión in situ típica, muchos hallazgos no pueden descubrirse hasta semanas, si no meses, después de que se hayan producido. Por ejemplo, un CRA informó de que se enteró de un embarazo no revelado —un evento grave de seguridad (SAE)— varios meses después de que se produjera debido a la falta de eSource para la supervisión remota.
Con Central eSource, el equipo de supervisión tiene acceso las 24 horas del día, los 7 días de la semana, a la fuente Clinicas, lo que permite una cadencia mucho más rápida y receptiva del SDR. Cuando se combina con herramientas RBQM basadas en estadísticas, Central eSource permite a los equipos clínicos detectar y prevenir desviaciones importantes mucho antes en el proceso, evitando problemas que podrían comprometer todo el estudio.
Resumen: Mucho más que poblar el EDC
En otra entrada del blog, demostramos que Central eSource tiene el potencial de realizar un mapeo de datos más preciso con el EDC que los sistemas fuente basados en EHR. Además de una mejor integración con el EDC, las ventajas descritas en este artículo son exclusivas de Central eSource:
| EHR | eSource Central | |
| Cumplimiento del protocolo | Sin impacto. Los sistemas EHR no se pueden configurar fácilmente para los requisitos específicos del estudio, por lo que el cumplimiento suele depender de la diligencia del coordinador a la hora de seguir las «hojas de flujo» en papel. | Alto. eSource se puede configurar para garantizar el cumplimiento del protocolo, minimizando los problemas de calidad de los datos. |
| Inicio del sitio y registro | Sin impacto. Los sistemas EHR no pueden heredar una plantilla de estudio diseñada de forma centralizada, por lo que cada centro debe desarrollar manualmente sus propios formularios específicos para cada protocolo. | Alto. Se puede crear una fuente electrónica diseñada de forma centralizada durante la fase de puesta en marcha y, a continuación, publicarla en Clinicas su activación, lo que elimina semanas de retraso. |
| Monitorización remota | Limitado. Algunos sistemas de EHR permiten el acceso remoto, pero en muchas ocasiones está restringido por tiempo y sujeto a complejos requisitos de acceso específicos del sitio. | Alto. Central eSource de CRIO incluye una herramienta de supervisión remota dedicada que permite revisar la fuente del sitio las 24 horas del día, los 7 días de la semana. |
