Más del 70 % de los datos de los ensayos clínicos actuales proceden de datos que no son formularios de informe de casos. Los datos que no son formularios de informe de casos incluyen datos continuos, como datos de dispositivos wearables, datos de laboratorio, datos comunicados por los pacientes y datos de ECG, por nombrar algunos. En términos generales, todos ellos se recopilan como fuente sin transcripción ni introducción en otro sistema. Hoy en día, hemos llegado a un punto crítico en el que podemos tomar decisiones activas sobre cómo evolucionará la gestión de datos. De lo contrario, serán fuerzas externas las que impulsen el cambio. Tras años de debate, ha llegado el momento de pasar de la gestión de datos a la ciencia de datos.
Según informa la Sociedad para la Gestión de Datos Clínicos en su reciente informe sobre innovación titulado «Las 5 V de la recopilación de datos clínicos»,el sector debe replantearse su enfoque y comprender cómo las 5 V de los datos están transformando la gestión de datos clínicos .
¿Qué son las 5 V?
Comencemos por definir las 5 V de los datos. El volumen, la variedad, la velocidad, la veracidad y el valor conforman los 5 elementos de los datos que vemos hoy en día en los ensayos clínicos.
Volumen
El volumen de datos en un ensayo de fase III ha aumentado exponencialmente durante la última década, pasando de millones de puntos de datos a miles de millones. Esto está directamente relacionado con el aumento de los datos de dispositivos portátiles/sensores, los datos del mundo real y el aumento de los datos de biomarcadores, por nombrar algunos.
Variedad
La variedad de datos recopilados hoy en día en los ensayos clínicos ha aumentado. Esto se ha acentuado significativamente debido a la pandemia y a la creciente adopción de herramientas y tecnologías por parte de compañías farmacéuticas impulsar enfoques más centrados en el paciente. Esto significa que, en la actualidad, cada vez se recopilan más datos de forma directa como fuente electrónica (eSource) en los ensayos clínicos.
Con esta variedad de datos, los autores del informe técnico sobre las 5 V indican que: «Esto significa que es necesario proporcionar información sobre la calidad y la integridad de los datos de esta variedad de fuentes electrónicas en el momento de la generación de los datos. Una vez generados los datos, el CDM rara vez podrá enviar una consulta para solicitar su corrección».
Velocidad
No hace falta decir que la velocidad y la intensidad de los datos que recopilamos hoy en día también han aumentado enormemente. Los dispositivos portátiles, los sensores y otras fuentes de datos continuas están aumentando su uso en determinadas áreas terapéuticas. Este aumento de la velocidad requiere la evolución de la gestión de datos hacia la ciencia de datos. La aplicación de la agregación de datos, el análisis y la evaluación de tendencias y valores atípicos es clave para la gestión de esta velocidad de datos.
Veracidad
The 5Vs white paper indicates that:“Often, veracity is associated with the key attributes of data integrity and ALCOA+ (Attributable, Legible, Contemporaneous, Original, Accurate, Complete, Consistent, Enduring, and Available). Veracity also can be associated with some of the attributes of data quality such as data conformity, credibility, and reliability. <Because of this, organizations> must establish proactive measures to secure the authenticity and security of the data. This is becoming critical in the world of e-Source and Real World Data, where data can rarely be corrected and where anonymization is increasingly challenging and critical.”
Valor
En el entorno actual de los ensayos clínicos, nos vemos inundados de datos. ¿Son valiosos estos datos? ¿Aportan algún valor añadido las comprobaciones de edición y lógicas que programamos? El informe técnico sobre las 5 V fomenta la maximización del valor relativo de un punto de datos específico. Al pasar de la gestión tradicional de datos a la ciencia de datos, la quinta V de las 5V, el valor, insta a la industria a considerar el hecho de que el valor de los datos va más allá de la integridad y la calidad. Al planificar sus ensayos clínicos, es importante tener en cuenta y comprender todo el potencial y el valor de los datos. La ciencia de datos clínicos se encuentra en la intersección de garantizar que todas las partes interesadas obtengan lo que necesitan para tener éxito.
¿Qué significa pasar de la gestión de datos a la ciencia de datos?
compañías farmacéuticas las CRO deben adoptar un verdadero modelo de fuentes electrónicas en todos los datos.
¿Y si pudiera acceder a una red de casi 2000 Clinicas de investigación Clinicas ya cuentan con tecnología, están orientadas al paciente, se preocupan por la calidad y son líderes en diversidad, equidad e inclusión? Y, mejor aún, ¿y si pudiera aprovechar los datos que estas Clinicas incluidos los proveedores de atención médica a domicilio y otros actores no tradicionales, como las cadenas de farmacias) ya están recopilando sin necesidad de utilizar una herramienta de recopilación de datos adicional?
Dejen de imponer tecnología innecesaria y costosa a Clinicas
Muchas Clinicas de investigación ya Clinicas adoptado la tecnología para realizar estudios recopilar datos. compañías farmacéuticas revisar y supervisar activamente los datos recopilados mediante esta tecnología. Sin embargo, muchas compañías farmacéuticas innumerables horas y enormes cantidades de dinero a herramientas de terceros que obligan Clinicas volver a introducir datos que ya han recopilado. De hecho, los usuarios de los centros son los únicos usuarios de todo el proceso de investigación que no tienen voz ni voto sobre la tecnología que utilizan en su trabajo diario.
Fuente electrónica basada en protocolos
compañías farmacéuticas las CRO pueden utilizar CRIO para definir plantillas eSource específicas para cada estudio. Estas se derivan directamente del protocolo. Es importante destacar que estas plantillas se ordenan de acuerdo con el calendario de evaluaciones. Las plantillas eSource de CRIO constituyen la base de lo que se envía tanto a Clinicas CRIO preexistentes como a Clinicas nuevas. Por último, estas plantillas eSource servirán para recopilar datos que cumplan con el protocolo.
Además, Clinicas crear e incluir sus propios procedimientos específicos, además de los proporcionados por el patrocinador. Este enfoque garantiza una recopilación de datos conforme al protocolo en el momento de la consulta del paciente. También incluye comprobaciones de validación en tiempo real para interrogar los datos en el momento de su introducción. Este enfoque conduce a una mejor calidad, menos consultas posteriores a la introducción de datos, un mayor cumplimiento del protocolo y una serie de eficiencias en el proceso. En consecuencia, esto permite a Clinicas disponer de Clinicas tiempo para centrarse en los aspectos críticos del ensayo, como el reclutamiento, la retención, el seguimiento de los pacientes y la responsabilidad sobre los medicamentos del estudio.
Con 2000 Clinicas CRIO eSource en casi 5000 protocolos activos, CRIO cuenta ahora con una gran base de datos para cuantificar el impacto en el rendimiento de los centros. Nuestros estudios de casos estudios nuestra investigación cuantitativa demuestran que Clinicas reducir las desviaciones de los protocolos en un 40 % y disminuir el riesgo de un resultado negativo en la auditoría de la FDA en un 70 % cuando utilizan CRIO. Además, hemos demostrado que Clinicas utilizan CRIO superan a Clinicas no lo Clinicas la inscripción en 2 de cada 3 ensayos, con un rendimiento medio superior del 40 %. Por último, en toda la red de centros CRIO, observamos una diversidad racial que duplica la media del sector.
Utilice eSource para impulsar la evolución desde la gestión de datos hasta la ciencia de datos.
El sistema de CRIO puede enviar automáticamente los datos eSource del centro directamente a una aplicación orientada al patrocinador llamada Reviewer EDC, que permite al equipo clínico revisar los datos de forma remota. Gracias a las comprobaciones de edición integradas en el sistema en el momento de la captura, es más probable que los datos se introduzcan en el sistema de forma precisa y completa. Dado que ahora los datos eSource son efectivamente los mismos que los datos eCRF, no es necesario realizar el seguimiento tradicional in situ ni la verificación de los datos de origen.
En este marco, compañías farmacéuticas las CRO deben adoptar un enfoque centralizado de supervisión de datos clínicos. Esto proporciona un único flujo de trabajo principal para la supervisión clínica y la revisión de los datos a medida que se introducen. En este flujo de trabajo, los equipos de supervisión pueden revisar los datos, emitir y cerrar consultas, realizar un seguimiento de los cambios en los datos de origen, bloquear datos y codificar médicamente términos literales. Esto agiliza el enfoque de revisión y gestión de datos, eliminando la revisión redundante de datos. La siguiente figura muestra cómo los cinco flujos de trabajo tradicionales pueden simplificarse en un flujo de trabajo rediseñado.
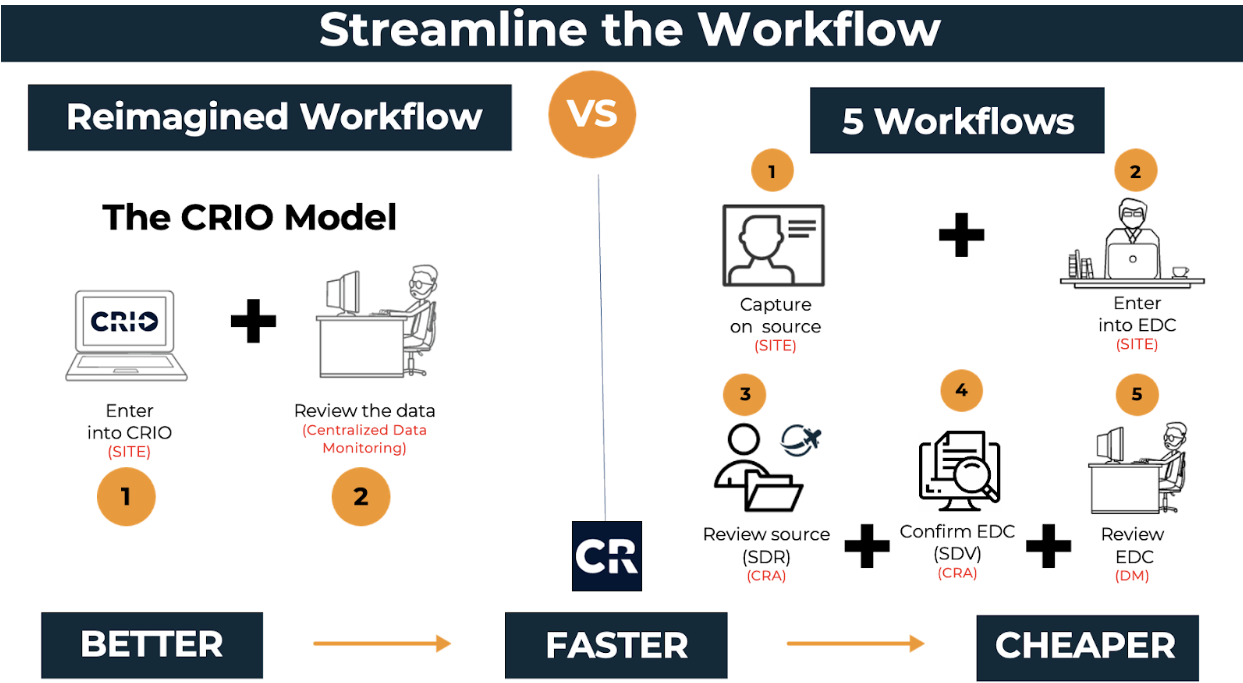
compañías farmacéuticas replantearse el proceso de los ensayos clínicos y aprovechar lo que está a la vista de todos:
El doble enfoque de CRIO para abordar las necesidades de Clinicas compañías farmacéuticas valor para ambas partes interesadas, reduciendo el número de sistemas redundantes y administrativamente onerosos que se imponen a Clinicas aumentando la eficiencia en términos de costes y tiempo.
La gestión de datos debe evolucionar para convertirse en ciencia de datos.
Para establecer un equipo central de supervisión de datos clínicos cohesionado, debemos eliminar las barreras y la segmentación entre departamentos. Es fundamental armonizar las diversas funciones y tareas de la codificación médica, los supervisores de datos clínicos y los científicos de datos, bajo un enfoque unificado. Si se hace correctamente, esto respaldará la evolución hacia la supervisión centralizada de datos y la ciencia de datos como enfoque principal para la supervisión y el control de datos.
En última instancia, aunque cada organización puede adoptar un enfoque ligeramente diferente a la hora de organizar el mejor modelo para garantizar la supervisión de la calidad de los datos, el libro blanco de la Sociedad para la Gestión de Datos Clínicos, titulado «Cómo crear una organización de ciencia de datos clínicos», anima a las organizaciones a que los profesionales de datos clínicos formen parte integral del enfoque de supervisión.
Desarrollar un plan integrado de gestión de datos clínicos.
Al fin y al cabo, se trata de gestionar los datos clínicos. Mediante el uso de herramientas como CRIO, compañías farmacéuticas las CRO pueden adoptar un enfoque integrado para la gestión de los datos clínicos. Al desarrollar y mantener un plan que reúna los elementos necesarios para la supervisión de los datos clínicos durante el inicio, la realización y el cierre del estudio, se puede esbozar y gestionar un enfoque más racionalizado. Es fundamental comprender y esbozar toda la revisión de datos necesaria, la seguridad de los pacientes y la supervisión de los datos en un plan integral. Un plan integrado permite una supervisión mejorada y directa de los elementos críticos de la supervisión de los pacientes y el control de la seguridad. Este enfoque integrado refuerza aún más el uso de CRIO para la captura directa de los datos de los pacientes. En conjunto, CRIO elimina las capas redundantes de revisión de datos al integrar la revisión de los datos de los pacientes en una única función integrada.
Además, gracias a este enfoque, los gestores de datos pueden liberarse de la innecesaria revisión formulario por formulario. Los profesionales de datos seguirán centrándose en el plan de gestión de datos y respaldarán el nuevo proceso de supervisión de datos clínicos mediante el suministro de listados, análisis de datos, tendencias y valores atípicos. CRIO permite un acceso mucho más preciso y contemporáneo a los datos de origen del centro. Esto permite a los profesionales de datos realizar mejores análisis y aumentar su inteligencia.
Es importante destacar que compañías farmacéuticas tienen que inventar un nuevo proceso. En su lugar, pueden utilizar un proceso que ya está disponible y a la vista de todos. La sociedad de gestión de datos y ciencia de datos más grande del mundo, SCDM, fomenta y respalda aún más este proceso. No se trata de un reto de invención, descubrimiento o incluso innovación. ¡Se trata de un reto de reinvención!
Lectura relacionada:Datos del pasado: de Triplicate a eCRF
