No mundo dos ensaios clínicos, a questão não é se irá enfrentar uma inspeção, mas sim quando. Quer seja um centro de ensaios, um promotor ou uma CRO, manter-se preparado para uma inspeção não se resume apenas à conformidade; trata-se de proteger a segurança dos participantes e garantir a integridade dos dados. Vamos explorar o que é necessário para responder com confiança «sim» quando se ouvir aquela batida à porta.
O que é a preparação para a inspeção?
A prontidão para inspeções é um estado contínuo de preparação que garante o cumprimento dos quadros regulamentares, incluindo as diretrizes ICH-GCP, os regulamentos da FDA (21 CFR Partes 11, 50, 54 e 312), o Regulamento da UE sobre Ensaios Clínicos (CTR) n.º 536/2014, o RGPD, os requisitos de BPC da MHRA, as diretrizes de BPC da OMS e outras normas aplicáveis. É a base que protege a segurança e o bem-estar dos participantes, mantendo simultaneamente a conformidade com os protocolos do estudo.
O que está em jogo é muito importante. De acordo com os dados das inspeções da FDA de 2024, o incumprimento do protocolo representa 55,4% das advertências aos investigadores, enquanto os registos inadequados da história clínica representam 24,1% das constatações. Estas estatísticas sublinham uma verdade fundamental: estar preparado não é apenas uma boa prática — é essencial para manter a integridade dos dados e evitar atrasos dispendiosos.
Compreender o processo de inspeção
Embora os procedimentos de inspeção variem consoante a autoridade reguladora, vários elementos fundamentais mantêm-se constantes:
- Notificação formal da autoridade reguladora a anunciar a próxima inspeção
- Reunião inicial para definir o âmbito do projeto e estabelecer expectativas claras
- Pedidos de documentos apresentados antes, durante ou após a inspeção
- Pedidos de acesso ao sistema que vão desde a visualização por cima do ombro até ao acesso direto através de contas dedicadas aos inspetores
Compreender este processo ajuda as organizações a prepararem-se de forma sistemática, em vez de terem de agir à pressa quando a notificação chega.
A vantagem tecnológica: por que razão os sistemas eletrónicos são importantes
Os dias em que era preciso vasculhar arquivos e pastas durante as inspeções estão a chegar ao fim. Os sistemas eletrónicos transformaram a preparação para as inspeções de um pesadelo logístico num processo simplificado.
Considere a diferença prática: um inspetor solicita todos os relatórios de eventos adversos dos últimos seis meses. Com sistemas em papel, isso implica vasculhar várias pastas, com o risco de perder documentos e desperdiçar tempo valioso da inspeção. Com um sistema eletrónico como o CRIO, basta alguns cliques — é instantâneo, completo e auditável.
Os sistemas eletrónicos oferecem vantagens evidentes:
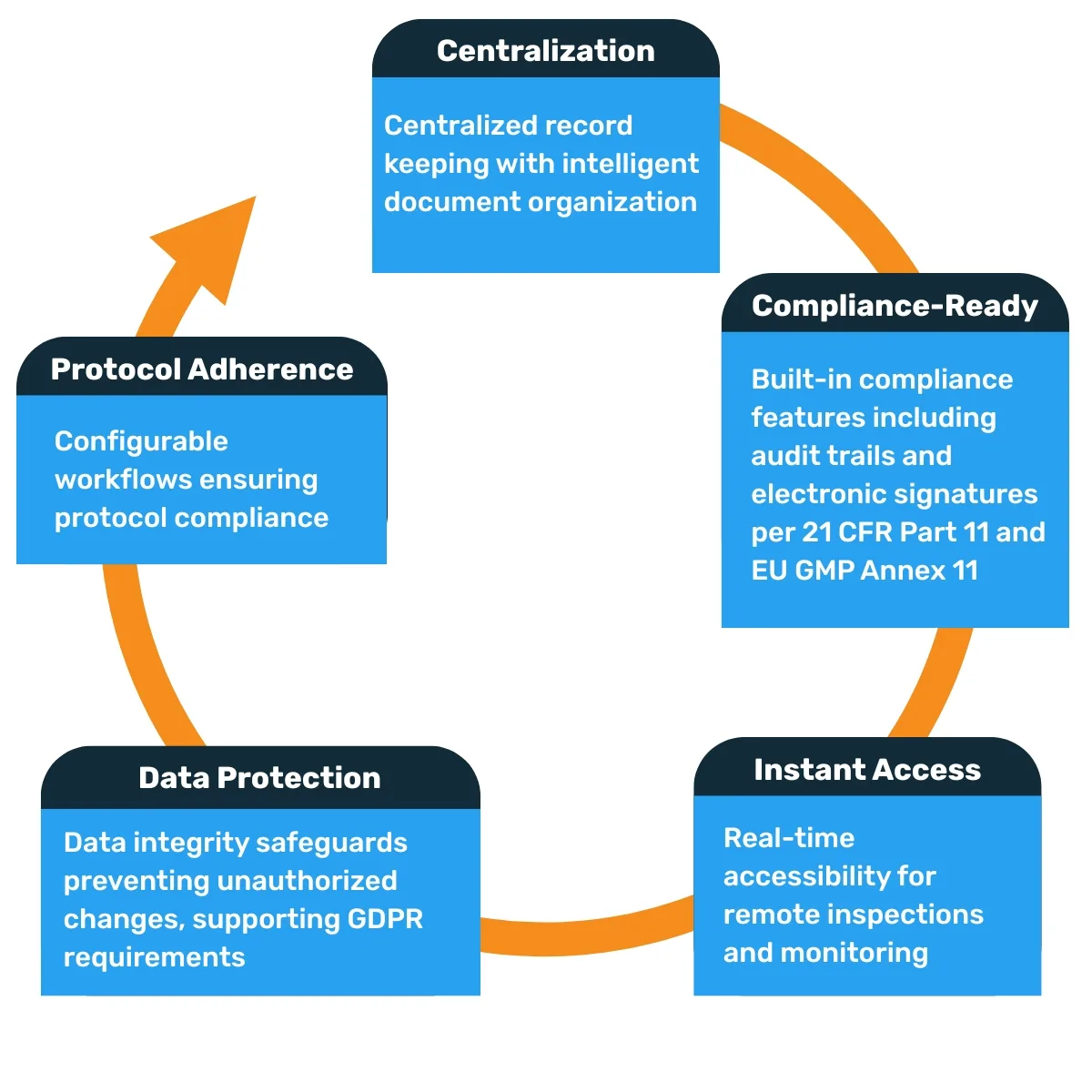
Acompanhar a evolução regulamentar
O panorama regulamentar evoluiu drasticamente, especialmente na sequência da pandemia. As orientações da FDA sobre a Avaliação Regulamentar à Distância (RRA) e a norma ICH E6(R3) demonstram a adesão das entidades reguladoras à tecnologia e às abordagens baseadas no risco.
Princípios fundamentais da norma ICH E6(R3) que apoiam a adoção de tecnologias:
- Neutralidade de meios: Escolha o sistema eletrónico mais adequado para a sua organização
- Flexibilidade e inovação: tirar partido dos dispositivos vestíveis, da monitorização remota e de abordagens inovadoras
- Qualidade proativa: integrar a qualidade nos processos desde o início
- Governança de dados: Garantir a recolha, o armazenamento e o acesso responsáveis aos dados, em conformidade com o RGPD (quando aplicável)
- Proporcionalidade do risco: Equilibrar a supervisão com a eficiência operacional
Como observou recentemente Jason Wakelin-Smith, da MHRA: «É chegado o momento de os patrocinadores adotarem a proporcionalidade do risco, sabendo que conta com o apoio das entidades reguladoras para a sua aplicação.»
Os nove pilares da preparação para a inspeção
Uma verdadeira preparação para a inspeção requer excelência em nove áreas críticas:
1. Conformidade regulamentar
Manter a conformidade com os regulamentos da FDA (21 CFR, Partes 11, 50, 54 e 312), as diretrizes da EMA, os requisitos de BPC da MHRA, as diretrizes de BPC da OMS e da ICH-GCP, bem como outros quadros normativos aplicáveis. Não se trata apenas de conhecer os regulamentos, mas sim de demonstrar uma aplicação consistente dos mesmos.
2. Documentação do estudo
Mantenha registos completos, precisos e atualizados, incluindo os ficheiros do centro de investigação (ISF), os documentos de origem e os formulários de relatório do investigador (CRF), em conformidade com os requisitos da norma 21 CFR Parte 312. A documentação deve refletir o desenrolar completo do seu ensaio clínico.
3. Formação e delegação
Certifique-se de que todo o pessoal recebe formação adequada, com registos documentados e registos claros de delegação, em conformidade com a norma 21 CFR Parte 312. Cada membro da equipa deve compreender as suas responsabilidades e limitações.
4. Segurança e direitos dos participantes
Implementar processos robustos de consentimento informado, em conformidade com o 21 CFR Parte 50, e manter sistemas que priorizem a segurança dos participantes acima de tudo. Assegurar a documentação adequada dos interesses financeiros, nos termos do 21 CFR Parte 54.
5. Gestão de produtos em fase de investigação
Assegure um armazenamento seguro através de controlos de temperatura adequados e registos de responsabilização meticulosos. Cada dose deve ser rastreável desde a receção até à eliminação, em conformidade com os requisitos da norma 21 CFR Parte 312.
6. Integridade dos dados
Garantir a introdução de dados precisa e atempada, a resolução rápida de questões e registos de auditoria exaustivos, em conformidade com as normas 21 CFR Parte 11 e do Anexo 11 das BPF da UE. Os dados devem estar em conformidade com o princípio ALCOA+: Atribuíveis, Legíveis, Contemporâneos, Originais, Precisos — além de Completos, Consistentes, Duradouros e Disponíveis. O tratamento de dados pessoais deve estar em conformidade com os requisitos do RGPD (quando aplicável).
7. Prontidão operacional
Estabeleça processos claros para a gestão das inspeções, com documentação facilmente acessível. A sua equipa deve saber exatamente o que fazer quando os inspetores chegarem.
8. Garantia de qualidade
Realizar auditorias internas regulares, implementar medidas de correção e prevenção (CAPA) de forma eficaz e manter abordagens de monitorização baseadas no risco, em conformidade com as diretrizes ICH E6(R3) e as diretrizes de Boas Práticas Clínicas (BPC) da OMS.
9. Tecnologia e Sistemas
Utilize sistemas validados, com uma supervisão adequada do fornecedor e testes de aceitação do utilizador documentados. A sua tecnologia deve facilitar, e não dificultar, o cumprimento dos princípios da norma 21 CFR Parte 11 e do Anexo 11 das BPF da UE.
Medidas práticas para alcançar a preparação
Põe estes princípios em prática com estes passos práticos:
Criar um plano de preparação do local: Elaborar uma lista de verificação abrangente que inclua todos os documentos essenciais. Atribuir responsabilidades claras pela manutenção de cada aspeto da preparação para a inspeção.
Implemente um sistema centralizado: quer seja físico ou eletrónico, mantenha um sistema de arquivo organizado que permita a rápida recuperação de qualquer documento que um inspetor possa solicitar.
Realize simulações de inspeções: as simulações regulares permitem identificar lacunas e reforçar a confiança da equipa. Leve-as a sério — são a sua melhor preparação para a situação real.
Criar uma equipa de resposta à inspeção: nomear um responsável pela inspeção e estabelecer protocolos de comunicação claros. Todos devem saber qual é o seu papel quando chegar o dia da inspeção.
Aposte na melhoria contínua: utilize os resultados das inspeções, sejam elas simuladas ou reais, como oportunidades de aprendizagem para reforçar os seus processos.
Considerações fundamentais para o sucesso

Evitar duas armadilhas críticas
Armadilha n.º 1: Supervisão inadequada do fornecedor Não presuma que o seu fornecedor está em conformidade — verifique-o. Solicite documentação abrangente de conformidade com a norma 21 CFR Parte 11, o Anexo 11 das BPF da UE e o RGPD antes da implementação, e não durante uma inspeção.
Armadilha n.º 2: Processos internos deficientes. Dispor de uma tecnologia de ponta não serve de nada sem processos claros para a sua utilização. Elabore orientações abrangentes para o pessoal e mantenha registos que comprovem que os sistemas funcionam conforme previsto.
Conclusão
A preparação para as inspeções não é um destino, mas sim um percurso de melhoria contínua. Ao adotar ferramentas eletrónicas que cumprem as normas 21 CFR Parte 11 e do Anexo 11 das BPF da UE, ao manter uma documentação abrangente e ao promover uma cultura de qualidade alinhada com as diretrizes das boas práticas clínicas, transforma as inspeções de eventos temidos em oportunidades para demonstrar a sua excelência.
Lembre-se de que, no fundo, a preparação para inspeções assenta em dois princípios fundamentais: proteger os participantes no estudo (21 CFR Parte 50) e garantir a integridade dos dados (21 CFR Parte 11, RGPD). Tudo o resto serve para apoiar estes objetivos essenciais.
A questão permanece: está preparado para uma inspeção de um ensaio clínico amanhã?
Com uma preparação adequada, a tecnologia certa e o compromisso com estes princípios, poderá responder com confiança «sim», não só amanhã, mas todos os dias.
Na CRIO, integramos a preparação para inspeções na base da nossa plataforma. O nosso centro de documentação abrangente, os certificados de validação e as funcionalidades de conformidade integradas ajudam os centros de ensaio, os patrocinadores e as CROs a manter a preparação para inspeções como um estado contínuo, e não como uma correria de última hora. Saiba mais sobre como garantir a preparação para inspeções com a CRIO em clinicalresearch.io.
