A sua plataforma eSource em conformidade com a norma 21 CFR Parte 11
É fácil presumir que os dados de investigação clínica residem nos registos de saúde eletrónicos (EHR) e só precisam de ser mapeados para o seu sistema de captura de dados eletrónicos (EDC). Mas os dados de investigação muitas vezes acabam em documentos em papel porque os sistemas EHR são projetados para capturar registos relacionados com diagnósticos e cuidados ao paciente, não com investigação.
Existe um software de investigação clínica comprovado que pode colmatar esta lacuna e aliviar os encargos da realização de investigação na sua instituição. É claramente o CRIO.
-
40% menos desvios do protocolo
-
70% menos risco de auditoria
Aprofunde-se nas diferenças entre EHR e eSource e como a CRIO preenche as lacunas.
Software intuitivo de investigação clínica que permite o cumprimento eficiente dos protocolos
Uma tecnologia eSource extremamente simples, criada por uma equipa de especialistas em investigação clínica, o CRIO ajuda-o a eliminar o papel, a tirar o máximo partido dos sistemas que já possui e a capacitar as suas equipas.
Colabore remotamente
- Colmatar as lacunas entre os sistemas de registos de saúde eletrónicos, os documentos originais em papel e o EDC
- Simplificar a revisão dos dados laboratoriais e registos médicos pelo investigador principal (PI)
- Forneça monitorização remota conveniente para assistentes de investigação clínica (CRAs), reduzindo simultaneamente a carga de trabalho do coordenador.
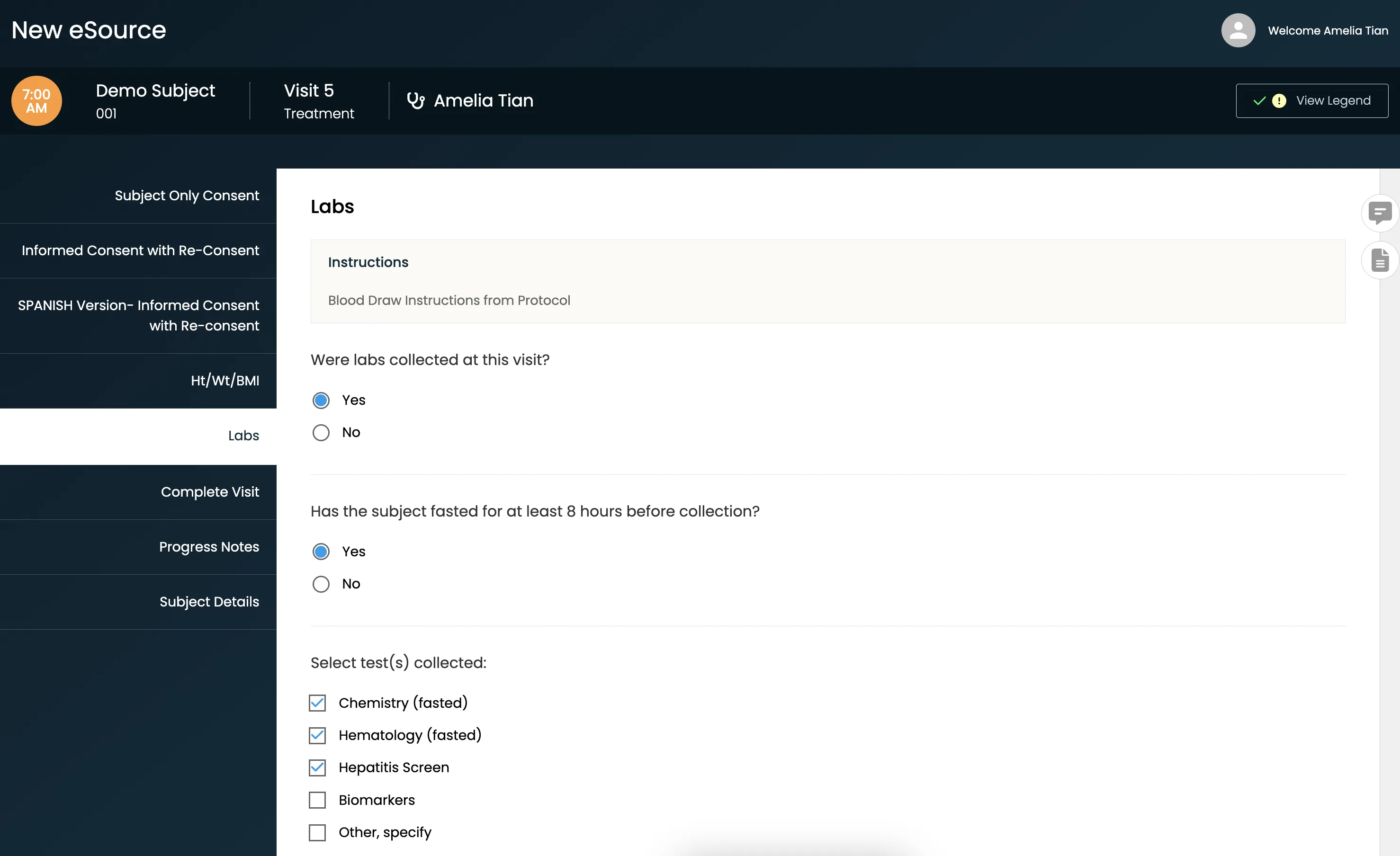
Realize facilmente ensaios clínicos iniciados por investigadores com EDC integrado
- Configure e implemente rapidamente modelos eSource sem quaisquer requisitos de programação
- Preencha automaticamente o EDC com dados protegidos por PHI à medida que preenche os modelos de origem, eliminando a transcrição e a verificação dos dados de origem (SDV).
- Suporte a ensaios clínicos em um único local e em vários locais, incluindo aqueles que exigem conformidade com a norma 21 CFR Parte 11
Proteger a segurança e a qualidade
- Cumpra as diretrizes de conformidade, incluindo 21 CFR Parte 11

Estudo de caso
Esta universidade economiza mais de 650 horas de trabalho do coordenador por ano
Veja por dentro o que acontece quando centros de pesquisa académica deixam de usar papel com o software CRIO eSource.