Atualmente, mais de 70% dos dados de ensaios clínicos provêm de fontes que não são formulários de relatório de caso. Esses dados incluem dados contínuos, tais como dados de dispositivos vestíveis, dados laboratoriais, dados relatados pelos doentes e dados de ECG, entre outros. De um modo geral, todos estes dados são recolhidos na sua forma original, sem transcrição ou introdução noutro sistema. Atualmente, chegámos a um ponto crítico em que podemos tomar decisões ativas sobre a forma como a gestão de dados irá evoluir. Caso contrário, serão forças externas a impulsionar a mudança. Após anos de discussão, chegou o momento da transição da gestão de dados para a ciência de dados.
Conforme relatado pela Society for Clinical Data Management no seu livro branco sobre inovação recentemente publicado, intitulado «Os 5Vs da recolha de dados clínicos»,o setor deve repensar a sua abordagem e compreender como os 5Vs dos dados estão a redefinir a gestão de dados clínicos.
O que são os 5V?
Comecemos por definir os 5V dos dados. Volume, variedade, velocidade, veracidade e valor constituem os 5 elementos dos dados que observamos atualmente nos ensaios clínicos.
Volume
O volume de dados num ensaio de Fase III aumentou exponencialmente na última década, passando de milhões para milhares de milhões de pontos de dados. Isto está diretamente relacionado com o aumento dos dados provenientes de dispositivos vestíveis e sensores, dos dados do mundo real e dos dados de biomarcadores, entre outros.
Variedade
A variedade de dados recolhidos atualmente nos ensaios clínicos tem vindo a aumentar. É importante referir que esta tendência foi acentuada pela pandemia e pela crescente adoção de ferramentas e tecnologias por parte dos patrocinadores, com o objetivo de promover abordagens mais centradas no doente. Isto significa que, nos ensaios clínicos atuais, se verifica cada vez mais a recolha direta de dados como fonte eletrónica (eSource).
Com esta variedade de dados, os autores do documento técnico sobre os 5Vs indicam que: «Isto significa que o feedback sobre a qualidade e a integridade dos dados desta variedade de fontes eletrónicas deve ser fornecido no momento da geração dos dados. Após a geração dos dados, o CDM raramente poderá enviar uma consulta para solicitar a sua correção.»
Velocidade
Escusado será dizer que a velocidade e a intensidade dos dados que recolhemos hoje também aumentaram consideravelmente. Os dispositivos vestíveis, os sensores e outras fontes de dados contínuos estão a ser cada vez mais utilizados em determinadas áreas terapêuticas. Este aumento da velocidade exige a evolução da gestão de dados para a ciência de dados. A aplicação da agregação de dados, da análise e da avaliação de tendências e valores atípicos é fundamental para a gestão desta velocidade de dados.
Veracidade
The 5Vs white paper indicates that:“Often, veracity is associated with the key attributes of data integrity and ALCOA+ (Attributable, Legible, Contemporaneous, Original, Accurate, Complete, Consistent, Enduring, and Available). Veracity also can be associated with some of the attributes of data quality such as data conformity, credibility, and reliability. <Because of this, organizations> must establish proactive measures to secure the authenticity and security of the data. This is becoming critical in the world of e-Source and Real World Data, where data can rarely be corrected and where anonymization is increasingly challenging and critical.”
Valor
No atual contexto dos ensaios clínicos, estamos inundados de dados. Estes dados são valiosos? As verificações de edição e de lógica que programamos acrescentam algum valor? O documento técnico sobre os 5V incentiva a maximização do valor relativo de um ponto de dados específico. Ao passar da gestão tradicional de dados para a ciência de dados, o 5.º V dos 5Vs, o valor, exorta a indústria a considerar o facto de que o valor dos dados vai além da integridade e da qualidade. Ao planear os seus ensaios clínicos, é importante considerar e compreender todo o potencial e valor dos dados. A ciência de dados clínicos situa-se na intersecção entre garantir que todas as partes interessadas obtenham o que precisam para serem bem-sucedidas.
O que significa passar da gestão de dados para a ciência de dados?
Os patrocinadores e as CROs precisam de adotar um verdadeiro modelo de eSource em todos os dados
E se pudesse aceder a uma rede de quase 2 000 centros de investigação que já estão equipados com tecnologia, orientados para o doente, focados na qualidade e são líderes em diversidade, equidade e inclusão? E, melhor ainda, e se pudesse aproveitar os dados que estes centros (incluindo prestadores de cuidados de saúde ao domicílio e outros intervenientes não tradicionais, como cadeias de farmácias) já estão a recolher, sem necessidade de uma ferramenta adicional de recolha de dados?
Deixem de impor tecnologias desnecessárias e dispendiosas aos sites
Muitos centros de investigação já adotaram a tecnologia para realizar estudos e recolher dados. Os patrocinadores podem analisar e monitorizar ativamente os dados recolhidos através desta tecnologia. No entanto, muitos patrocinadores gastam inúmeras horas e avultadas quantias de dinheiro em ferramentas de terceiros que obrigam os centros a voltar a introduzir dados que já tinham recolhido. Na verdade, os utilizadores dos centros são os únicos, em todo o processo de investigação, que não têm qualquer influência sobre a tecnologia que utilizam no seu trabalho quotidiano.
Fonte eletrónica orientada por protocolos
Os patrocinadores e as CROs podem utilizar o CRIO para definir modelos de eSource específicos para cada estudo. Estes modelos são derivados diretamente do protocolo. É importante referir que estes modelos são organizados de acordo com o calendário de avaliações. Os modelos de eSource do CRIO constituem, assim, a base do que é enviado tanto para os centros CRIO já existentes como para os novos. Por fim, estes modelos de eSource servirão para recolher dados em conformidade com o protocolo.
Além disso, os centros continuam a poder criar e incluir os seus próprios procedimentos específicos, para além do que é fornecido pelo promotor. Esta abordagem garante uma recolha de dados em conformidade com o protocolo no momento do contacto com o doente. Inclui também verificações de validação em tempo real para analisar os dados no momento da introdução. Esta abordagem conduz a uma melhor qualidade, a um menor número de consultas após a introdução de dados, a uma maior conformidade com o protocolo e a uma série de ganhos de eficiência nos processos. Consequentemente, isto proporciona aos centros mais tempo para se concentrarem nos aspetos críticos do ensaio, tais como o recrutamento, a retenção, o acompanhamento dos doentes e a responsabilização pelo medicamento em estudo.
Com 2.000 centros a utilizar o CRIO eSource em quase 5.000 protocolos ativos, a CRIO dispõe agora de uma vasta base de dados para quantificar o impacto no desempenho dos centros. Os nossos estudos de caso e investigação quantitativa comprovam que os centros podem reduzir os desvios aos protocolos em 40% e diminuir o risco de um resultado negativo numa auditoria da FDA em 70% quando utilizam o CRIO. Além disso, demonstrámos que os centros que utilizam o CRIO superam os centros que não o utilizam no recrutamento em 2 em cada 3 ensaios, com um desempenho superior médio de 40%. E, finalmente, em toda a rede de centros CRIO, estamos a observar uma diversidade racial que é o dobro da média do setor .
Utilize o eSource para impulsionar a evolução da gestão de dados para a ciência de dados
O sistema da CRIO pode enviar automaticamente os dados do eSource do centro de ensaio diretamente para uma aplicação destinada ao patrocinador, denominada Reviewer EDC, que permite à equipa clínica analisar os dados remotamente. Graças às verificações de edição integradas no sistema no momento da captura, é mais provável que os dados sejam introduzidos no sistema de forma precisa e completa. Uma vez que o eSource é agora, na prática, idêntico aos dados do eCRF, não há necessidade de monitorização tradicional no local nem de verificação dos dados de origem.
Neste contexto, os patrocinadores e as CROs devem adotar uma abordagem centralizada de monitorização de dados clínicos. Isto permite um único fluxo de trabalho principal para a supervisão clínica e a revisão dos dados à medida que estes são introduzidos. Neste fluxo de trabalho, as equipas de monitorização podem rever os dados, emitir e encerrar consultas, acompanhar alterações nos dados de origem, bloquear dados e codificar clinicamente termos textuais. Isto simplifica a abordagem de revisão e gestão de dados, eliminando revisões redundantes adicionais. A figura abaixo ilustra como os cinco fluxos de trabalho tradicionais podem ser simplificados num fluxo de trabalho repensado.
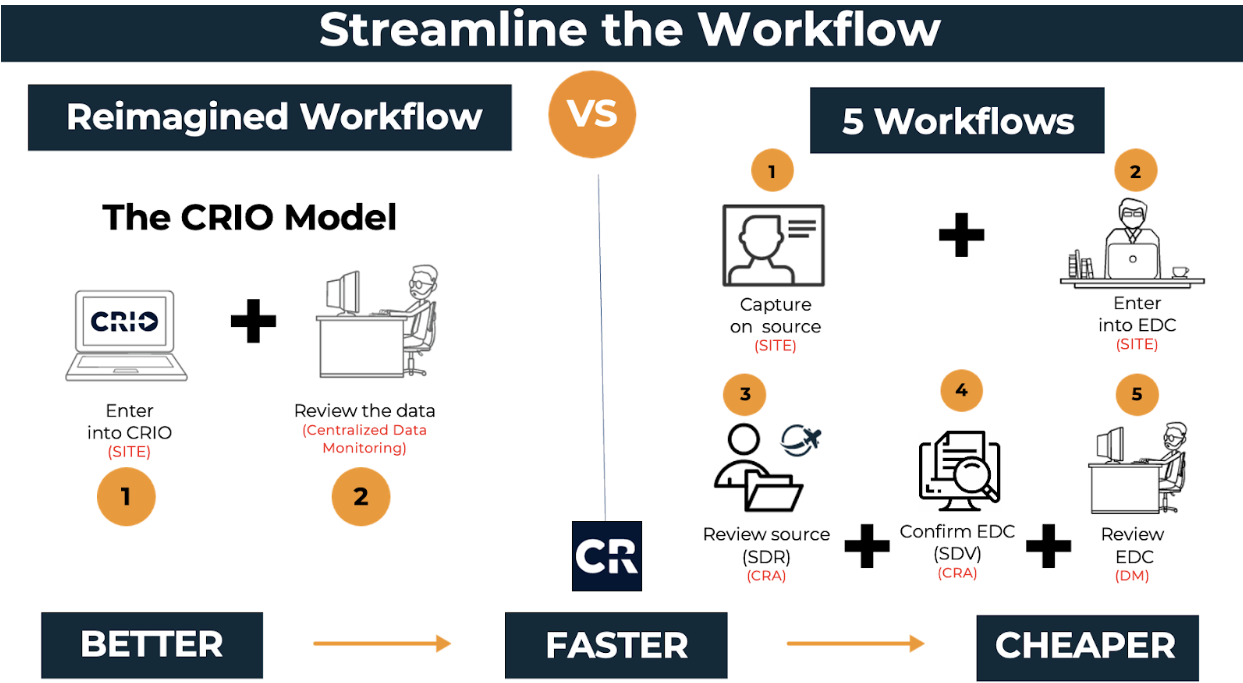
Os patrocinadores precisam de repensar o processo dos ensaios clínicos e tirar partido do que está à vista de todos:
A abordagem dupla da CRIO, que visa responder às necessidades dos centros de ensaio e dos patrocinadores, cria valor para ambas as partes interessadas, reduzindo o número de sistemas redundantes e administrativamente onerosos impostos aos centros de ensaio e promovendo ganhos de eficiência em termos de custos e tempo.
A gestão de dados deve evoluir para se tornar ciência de dados
Para criar uma equipa central de monitorização de dados clínicos coesa, temos de eliminar as barreiras e a fragmentação entre departamentos. É fundamental alinhar as diversas funções e responsabilidades da codificação médica, dos monitores de dados clínicos e dos cientistas de dados, no âmbito de uma abordagem unificada. Quando bem executado, isto irá apoiar a evolução no sentido da monitorização centralizada de dados e da ciência de dados como abordagem principal para a supervisão e monitorização de dados.
Em última análise, embora cada organização possa adotar uma abordagem ligeiramente diferente na definição do melhor modelo para garantir a supervisão da qualidade dos dados, o Livro Branco da Society for Clinical Data Management, intitulado «How to Create a Clinical Data Science Organization» (Como criar uma organização de ciência de dados clínicos), incentiva as organizações a integrar os profissionais de dados clínicos como parte integrante da abordagem de monitorização.
Elaborar um plano integrado de gestão de dados clínicos
No fim de contas, tudo se resume à gestão dos seus dados clínicos. Através da utilização de ferramentas como o CRIO, os patrocinadores e as CROs podem adotar uma abordagem integrada para a gestão de dados clínicos. Ao desenvolver e manter um plano que reúna os elementos necessários para a monitorização de dados clínicos durante o arranque, a condução e o encerramento do estudo, é possível delinear e gerir uma abordagem mais simplificada. É fundamental compreender e delinear toda a revisão de dados necessária, a segurança dos doentes e a supervisão dos dados num único plano abrangente. Um plano integrado permite uma supervisão melhorada e direta sobre os elementos críticos da supervisão dos doentes e da monitorização da segurança. Esta abordagem integrada reforça ainda mais a utilização do CRIO para a captura direta de dados dos doentes. Em suma, o CRIO elimina as camadas redundantes de revisão de dados, integrando a revisão dos dados dos doentes numa única função integrada.
Além disso, através desta abordagem, os gestores de dados podem ser libertados da revisão desnecessária, formulário a formulário. Os profissionais de dados continuarão a concentrar-se no plano de gestão de dados e a apoiar o novo processo de monitorização de dados clínicos através do fornecimento de listas, análises de dados, tendências e valores atípicos. O CRIO permite um acesso muito mais preciso e em tempo real aos dados de origem dos centros. Isto permite aos profissionais de dados realizar melhores análises e ampliar os seus conhecimentos.
É importante notar que os patrocinadores não precisam de inventar um novo processo. Em vez disso, podem recorrer a um processo que já está disponível e à vista de todos. A SCDM, a maior sociedade mundial de gestão de dados e ciência de dados, incentiva e apoia ainda mais este processo. Não se trata de um desafio de invenção, descoberta ou mesmo inovação. Trata-se de um desafio de reimaginação!
Leitura relacionada:Uma viagem ao passado dos dados: do formulário em triplicado ao eCRF
